HỘI CHỨNG SUY HÔ HẤP CẤP TIẾN TRIỂN
HỘI CHỨNG SUY HÔ HẤP CẤP TIẾN TRIỂN
I. Đại cương
Hội chứng suy hô hấp cấp tiến triển (Acute respiratory distress syndrome – ARDS) là hội chứng suy hô hấp cấp giảm oxy máu nặng đe dọa tính mạng bệnh nhân (BN), do nhiều nguyên nhân gây ra, có điểm chung là phản ứng viêm tại phổi gây tăng tính thấm thành mạch, tổn thương hàng rào phế nang mao mạch, dẫn đến phù mô kẽ và ngập lụt phế nang.
II. Nguyên nhân
2.1 Bệnh lý gây tổn thương phổi trực tiếp
– Viêm phổi nặng: là nguyên nhân thường gặp nhất, viêm phổi do vi khuẩn (phế cầu, liên cầu…), hoặc do virus (cúm A H5N1, SARS…).
– Hít dịch vị vào phổi: thường gặp trên BN hôn mê hoặc say rượu.
– Dập phổi.
– Thuyên tắc mỡ, khí , ối.
– Ngạt nước.
– Hít khí độc.
– Tiêm, hít heroin hay sử dụng các loại thuốc ma túy khác (cocain, amphetamin…).
– Phù phổi sau tái tưới máu: sau ghép phổi hoặc lấy huyết khối động mạch phổi.
2.2 Bệnh lý toàn thân gây tổn thương phổi gián tiếp
– Nhiễm khuẩn nặng hoặc sốc nhiễm khuẩn.
– Chấn thương nặng (đặc biệt khi có sốc và truyền nhiều máu).
– Thời gian tiến hành tim phổi nhân tạo kéo dài.
– Viêm tụy cấp nặng.
– Sốc không phải do tim (sốc phản vệ.).
– Bỏng nặng.
– Viêm mạch máu phổi.
– Truyền máu và các chế phẩm của máu: chẩn đoán ARDS do truyền máu và chế phẩm khi BN khởi phát cấp (trong hoặc trong vòng 6 giờ sau khi truyền) tình trạng giảm oxy máu (PaO2/FiO2 < 300mmHg hoặc SpO2 < 90mmHg với thở khí phòng), thâm nhiễm phế nang 2 bên không phải do suy tim hoặc quá tải dịch, không bị ARDS trước đó. Nếu có yếu tố nguy cơ chó ARDS lúc truyền thì chỉ chẩn đoán có khả năng ARDS do truyền máu.
– Quá liều thuốc.
III. Chẩn đoán:
3.1 Lâm sàng:
Các đặc điểm lâm sàng của ARDS thường xuất hiện trong vòng 6-72 giờ sau khi có yếu tố khởi phát và tiến triển xấu đi rất nhanh. Các biểu hiện thông thường gồm:
– Khó thở, thở nhanh, co kéo cơ hô hấp phụ, tím môi đầu chi, không đáp ứng với oxy liều cao.
– Nghe phổi có ran ẩm, nổ lan toả, có thể kèm với ho và đau ngực.
– Nhịp tim nhanh.
– Kèm theo các biểu hiện của yếu tố khởi phát.
3.2 Cận lâm sàng:
– Chẩn đoán hình ảnh: trên X- phổi có hình ảnh thâm nhiễm phế nang 2 bên, trên CT thấy đám mờ rải rác lan rộng hoặc tụ lại thành những vùng đông đặc, các hình ảnh này xuất hiện chủ yếu ở vùng thấp (dependent lung zones). Hình ảnh thâm nhiễm không nhất thiết phải lan toả và tầm trọng, chỉ cần thâm nhiễm 2 phế trường ở bất kỳ mức độ nào là đủ.
– Khí máu động mạch (KMĐM): biểu hiện của giảm oxy máu nặng, mức chênh lệch áp lực oxy giữa phế nang và mạch máu lớn, thường có kiềm hô hấp giai đoạn sớm và toan hô hấp giai đoạn muộn hơn.
3.3 Chẩn đoán xác định:
Tiêu chuẩn chẩn đoán được cập nhật vào 6/2012 bởi ATS (American Thoracic Society) và ESICM (European Society of Intensive Care Medicine):
1) Thời gian: triệu chứng hô hấp phải xuất hiện trong vòng 1 tuần sau 1 tổn thương trên lâm sàng đã biết có nguy cơ gây ARDS hoặc mới xuất hiện hoặc tiến triển xấu đi trong vòng 1 tuần trước đó.
2) Hình ảnhXQ: những đám mờ 2 bên phù hợp với phù phổi mà không giải thích được bằng tràn dịch, xẹp thùy phổi /xẹp phổi hoặc tổn thương dạng nốt trên phim XQ tim phổi thẳng hoặc CT ngực.

Hình CT: ARDS do sepsis sau viêm phổi do phế cầu khuẩn
Hình XQ: thâm nhiễm 2 bên, lan toả, bóng tim không to trên BN ARDS
3) Suy hô hấp mà không thể giải thích đầy đủ bằng tình trạng suy tim hoặc quá tải dịch. Một đánh giá khách quan (ví dụ: siêu âm tim) phải được làm để loại trừ phù phổi thuỷ tĩnh nếu không có yếu tố nguy cơ ARDS.
4) Sự oxy hoá máu
+ Nhẹ: 200 mmHg < PaO2/FiO2 ≤ 300 mmHg với mức PEEP hoặc CPAP ≥ 5 cmH2O.
+ Trung bình: 200 mmHg <PaO2/FiO2 ≤ 300 mmHg với PEEP hoặc CPAP ≥ 5 cmH2O.
+ Nặng: PaO2/FiO2 ≤ 100 mmHg với PEEP hoặc CPAP ≥ 5 cmH2O.
Chú ý: nếu không đo được KMĐM, có thể tạm dùng tỷ số SpO2/FiO2, với trị số 315 tương đương với 300 khi dùng PaO2/FiO2. Độ nhậy là 91%, độ đặc hiệu là 56%.
3.4 Chẩn đoán phân biệt
– Phù phổi cấp do tim
– Chảy máu phế nang lan tỏa
– Viêm phổi kẽ cấp tính
– Hội chứng Hamman-rich
– Viêm phổi cấp tăng bạch cầu ái toan
– Lao kê
– Viêm phổi tổ chức hóa không rõ căn nguyên
– Ung thư di căn lan tỏa
3.5 Chẩn đoán biến chứng chấn thương áp lực
Tràn khí trung thất, tràn khí màng phổi, tràn khí dưới da. Chiếm tỉ lệ 12-13%.
Viêm phổi bệnh viện
Chiếm tỉ lệ 15-60%. Rất khó chẩn đoán viêm phổi bệnh viện trên BN ARDS mà không do viêm phổi.
Các dấu hiệu gợi ý như: thâm nhiễm phổi mới hoặc tiến triển kèm sốt, bạch cầu tăng, đàm mủ.
Suy đa cơ quan
Là biến chứng thường gặp. Suy đa cơ quan có thể do bệnh lý gốc gây ra hoặc xảy ra độc lập. Tình trạng suy đa cơ quan gây khó khăn cho việc xác định chính xác nguyên nhân tử vong ở BN ARDS.
Tỉ lệ sống ở BN ARDS phụ thuộc vào khả năng điều trị nâng đỡ tình trạng suy đa cơ quan.
Yếu cơ
BN ARDS có nguy cơ rất cao bị yếu cơ kéo dài sau khi tổn thương phổi đã phục hồi gây khó khăn cho việc cai máy thở.
Hội chứng lâm sàng này thường được gọi là bệnh đa dây thần kinh ở BN nặng. thường gặp trên BN điều trị bằng steriod và thuốc giãn cơ.
Biến chứng khác
– Huyết khối tĩnh mạch sâu.
– Xuất huyết tiêu hóa do stress.
– Suy dinh dưỡng.
– Nhiễm trùng liên quan catheter.
4. Điều trị:
Bao gồm điều trị điều trị hỗ trợ, điều trị bệnh nguyên phát, điều trị biến chứng. Các biện pháp điều trị đặc hiệu chưa mang lại kết quả khả quan, nên chưa được khuyến cáo sử dụng thường quy trên lâm sàng.
4.1 Điều trị hỗ trợ:
Điều trị hỗ trợ bao gồm điều trị giảm oxy máu, dùng thuốc an thần – giảm đau -giãn cơ, kiểm soát dịch và huyết động, hỗ trợ dinh dưỡng, kiểm soát đường máu, điều trị viêm phổi bệnh viện, phòng ngừa huyết khối tĩnh mạch sâu và xuất huyết tiêu hoá.
4.1.1 Điều trị giảm oxy máu
Mục tiêu: PaO2: 55 – 80mmHg SpO2 88 – 95%. Các biện pháp gồm:
– Dùng FiO2 cao: mask không thở lại cung cấp FiO2 60 – 70%, thở máy xâm lấn có thể cung cấp FiO2100%. FiO2 > 50% gây độc, vì vậy, điều chỉnh FiO2 < 60% càng sớm càng tốt.
– Giảm tiêu thụ oxy: hạ sốt, giảm lo lắng, giảm đau, giảm hoạt động cơ hô hấp bằng thuốc hạ sốt, thuốc an thần – giảm đau – giãn cơ…
– Cải thiện cung cấp oxy cho mô: hạn chế dịch, nếu cần dùng lợi tiểu để giảm phù phổi, cho BN nằm sấp, truyền máu nếu Hb < 7 g/dL…
– Thở CPAP, thở máy không xâm lấn, thở máy xâm lấn.
4.1.2 Thông khí cơ học:
Hầu hết BN ARDS cần phải đặt nội khí quản (NKQ) – thở máy. Thở máy có thể gây ra tổn thương phổi, vì vậy, khi tiến hành thở máy phải cân bằng giữa mục tiêu oxy hóa máu phải đạt và hạn chế tối đa tổn thương phổi thêm vào.
Các mục tiêu cần đạt:
– Mục tiêu oxy hóa máu: PaO2: 55 – 80mmHg hoặc SpO2 88 – 95% (ưu tiên sử dụng PaO2 hơn SpO2).
– Mục tiêu hạn chế tổn thương phổi:
+ Vt thấp: 6mL/kg cân nặng.
+ Áp lực bình nguyên:Pplateau ≤ 30 cmH2O và càng thấp càng tốt (trong mode thể tích, muốn đo
Pplateau thì phải cài thời gian dừng cuối thì thở vào là 0.5 giây).
+ Chọn mức PEEP tối ưu để tránh xẹp phế nang theo chu kỳ thở.
+ FiO2 < 60% (có tài liệu < 70%).
+ Khí máu động mạch: pH 7.30 – 7.45
– Chấp nhận một số chỉ số sinh lý bên ngoài giới hạn bình thường:
+ Permissive hypoxemia: oxy máu chỉ cần đạt PaO2 > 55 mmHg, SaO2 88 – 95%
+ Permissive hypercapnia: cho phép tăng CO2 và chấp nhận toan hô hấp, nếu pH < 7.15 mà không thể tăng Vt thêm vì Pplat sẽ > 30, đồng thời tần số hô hấp cũng đã tăng đến 35l/ph → cho phép truyền kiềm giữ pH > 7.15 Các chiến lược thở máy hiện tại:
– Thông khí bảo vệ phổi (lung protective ventilation): Vt thấp
– Thông khí phổi mở (Open lung ventilation): Vt thấp + PEEP tối ưu.
– Thông khí với mức PEEP cao ( high positive end-expiratory pressure).
– Các biện pháp phụ trợ: huy động phế nang, thông khí cho BN nằm sấp, thở máy tần số cao, thông khí với I/E đảo ngược.
Thông khí bảo vệ phổi (lung protective ventilation):
Cài đặt ban đầu:
– Phương thức hỗ trợ/kiểm soát thể tích (Volume Assist/Control, V – A/C)
– Cài đặt Vt:
+ Tính trọng lượng lý tưởng (predicted body weight – PBW):
• PBW Nam = 50 + 0,91 [chiều cao (cm) – 152,4]
• PBW Nữ = 45,5 + 0,91 [chiều cao (cm) – 152,4]
• Hoặc PBW = 90% (chiều cao tính bằng cm – 100)
+ Đầu tiên để Vt 8mL/kg PBW. Sau đó, giảm xuống 7 rồi xuống 6mL/kg PBW trong vòng 1 – 3 giờ.
– Tần số thở: cài đặt < 35l/ph, sao cho phù hợp thông khí phút nền của BN.
– Dạng sóng dòng khí : giảm dần.
– I/E = 1/1 – 1/3
– PEEP và FiO2 cài đặt phối hợp theo ARDS Network.
Bảng phối hợp điều chỉnh PEEP và FiO2 theo ARDS Network
(để đạt mục tiêu oxy máu: PaO2 55-80mmHg hoặc SpO2 88-95%)
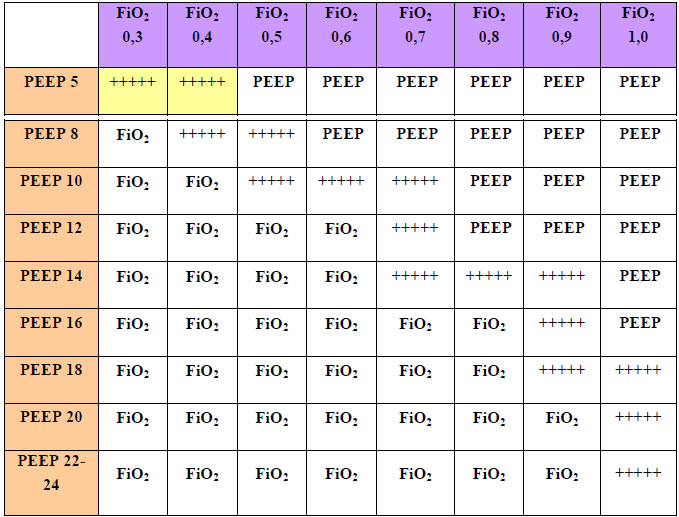
(+++++): là mức chấp nhận được của PEEP và FiO2
❖ Ví dụ: ban đầu để PEEP = 5 và FiO2 100%
– Nếu PaO2 < 55 mmHg hoặc SpO2 < 88%
+ Tăng PEEP dần lên theo bảng (tối đa là 18 cmH2O) tới khi PaO2 > 80 mmHg hoặc SpO2 > 95%. Sau đó giảm dần FiO2, để tới được vùng (+++++) mà vẫn duy trì được PaO2 > 55mmHg và SpO2 >88%. Nếu giảm chưa tới vùng (+++++), mà không giữ được PaO2 và SpO2 ta lại tăng dần PEEP lên để tới được vùng (+++++) mà vẫn duy trì được PaO2 >55 mmHg và SpO2 >88%. Sau đó điều chỉnh PEEP và FiO2 theo vùng (+++++).
+ Nếu PEEP đã là 18 và FiO2 = 100% mà không giữ được PaO2 > 55 mmHg hoặc SpO2 > 88%, tiếp tục tăng PEEP theo bảng [vùng (+++++)]
– Nếu PaO2 > 80mmHg và SpO2 > 95%
+ Giảm dần FiO2 theo bảng (xuống tối thiểu 40%) tới khi PaO2 < 55mmHg hoặc SpO2 < 88%. Lúc này tăng dần PEEP lên để tới được vùng (+++++) và duy trì được PaO2 > 55mmHg và SpO2 > 88mmHg. Sau đó điều chỉnh PEEP và FiO2 theo vùng (+++++).
Điều chỉnh máy thở:
– Theo dõi SpO2 (hoặc làm khí máu động mạch) và Pplat mỗi 4 giờ 1 lần (phải cài Pipause = 0.5s) và sau 1 – 5 phút điều chỉnh PEEP hoặc Vt.
– Điều chỉnh thông số máy thở theo các mục tiêu lần lượt là Pplateau, pH, oxy hoá máu.
❖ Điều chỉnh Vt theo mục tiêu Pplat < 30 cm H2O:
– Nếu Pplat > 30 cm H2O, giảm Vt đi 1 mL/kg PBW xuống 5 mL/kg PBW, hoặc nếu cần thiết để 4 mL/kg PBW.
– Nếu Pplat < 25 cm H2O và Vt < 6 mL/kg PBW, tăng Vt 1 mL/kg PBW cho đến khi Pplat > 25 cm H2O hoặc Vt = 6 mL/kg.
– Nếu BN có nhịp thở dồn dập hoặc khó thở nhiều, Vt có thể tăng lên đến 7 hoặc 8 mL/kg PBW nếu Pplat vẫn ≤ 30 cm H2O.
❖ Điều chỉnh Vt và F để đạt mục tiêu pH 7.30 – 7.45:
Điều chỉnh toan hô hấp:
– Nếu pH 7.15 – 7.30: tăng F đến khi pH ≥ 7.3 hoặc PaCO2 < 25; F tối đa 35l/ph.
– Nếu pH < 7.15 → tăng F đến 35 l/ph. Nếu vẫn còn < 7.15 → xem xét truyền natribicarbonat 8.4% 10 – 20 mL/giờ, Vt có thể tăng từng 1mL/kg cho đến khi pH > 7.15 (tối đa 8mL/kg), nếu tăng Vt mà Pplateau > 30 → xem xét mở phổi.
– Chấp nhận tăng PaCO2 miễn là vẫn đảm bảo được mục tiêu oxy hóa máu và áp lực bình nguyên ≤ 30. Trong trường đã điều chỉnh thở máy theo nhiều cách khác nhau mà vẫn không đảm bảo được mục tiêu oxy hóa đặt ra có thể cho BN nằm sấp, thông khí với tỉ lệ I/E đảo ngược, thông khí tần số cao hay trao đổi oxy qua tuần hoàn ngoài cơ thể (ECMO).
Điều chỉnh kiềm hô hấp (pH > 7.45):
– Mục tiêu đầu tiên là để Vt 6 mL/kg rồi giảm F.
– Chú ý: điều chỉnh F để tăng thông khí hay giảm thông khí chỉ được nếu BN hoàn toàn thở theo tần số máy. Điều này khó đạt được trong thực tế, BN ARDS thường thở nhanh 40 – 50l/ph mà không theo tần số máy cài đặt. Vì vậy, thường phải dùng an thần – giảm đau – giãn cơ mạnh để đè sập nhịp thở của BN.
❖ Điều chỉnh theo mục tiêu oxy hoá máu: PaO2 55-80 mmHg hoặc SpO2 88-95%.
– Ưu tiên sử dụng PaO2, sau đó mới là SpO2.
– Sử dụng “Bảng phối hợp FiO2 và PEEP” ở trên để đạt được mục tiêu.
– Ngoại lệ
+ Chấp nhận SpO2 < 88 hoặc > 95 trong thời gian ngắn (< 5 phút) mà không cần thay đổi thông số FiO2 và PEEP.
+ FiO2 = 1.0 có thể được sử dụng trong thời gian ngắn (< 10 phút) để chống thiếu oxy cấp nguy hiểm khi hút đàm.
+ Nếu Pplat > 30 và oxy hoá máu không đạt mục tiêu và Vt = 4 ml/kg, KHÔNG ĐƯỢC TĂNG PEEP, thì phải tăng FiO2 với mức tăng là 0.1 cho tới khi đạt được mục tiêu oxy hoá máu hoặc FiO2 = 1.0. Sau khi đã tăng FiO2 tới tối đa (1.0) mà vẫn chưa đạt được mục tiêu oxy hoá máu, thì tăng dần PEEP với mức tăng là 2 cmH2O/lần. Pplat có thể vượt quá 30 cmH2O trong trường hợp này.
+ Nếu FiO2 = 1.0; PEEP = 24, và mục tiêu oxy hoá máu chưa đạt được, thực hiện “thử nghiệm tăng PEEP” hoặc thủ thuật huy động phế nang.
❖ Thử nghiệm tăng PEEP
+ Tăng PEEP với mức tăng bằng 2 cm H2O cho tới tối đa là 34 hoặc khi đã đạt được mục tiêu oxy hoá máu.
+ Nếu tăng PEEP tới mức tối đa không hiệu quả trong vòng 4 giờ (PaO2 tăng lên < 5) thì hạ PEEP về mức 24.
+ Chú ý theo dõi phát hiện để xử trí kịp thời các biến chứng của các biện pháp trên: tràn khí màng phổi, truỵ mạch.
Thông khí phổi mở (Open lung ventilation):
– Có tác dụng mở các phế nang xẹp (làm giảm căng giãn phế nang do khí sẽ được chia sẻ bớt vào các phế nang này trong thì thở vào) và giảm đóng mở phế nang theo chu kỳ thở → giảm tổn thương phổi.
– Áp dụng cài đặt Vt như trên.
– Chọn PEEP tối ưu theo 2 cách:
+ Tìm điểm uốn thấp (lower inílection point) dựa vào đường cong áp lực – thể tích, sau đó đặt PEEP cao hơn điểm uốn thất ít nhất 2cm. Nếu không chắc chắn đâu là điểm uốn thấp thì để PEEP = 16 cmH2O.
+ Áp dụng thủ thuật huy động phế nang, sau thủ thuật để PEEP = 20, sau đó giảm dần PEEP mỗi 5 phút 1cmH2O cho đến khi compliance phổi tĩnh giảm nhiều và/hoặc PaO2 giảm 10% so với mức trước đó. Cài đặt PEEP cao hơn mức PEEP này 2cmH2O sau khi đã huy động phế nang lại 1 lần nữa.
Thông khí với mức PEEP cao ( high positive end-expiratory pressure):
– Cũng là thông khí phổi mở nhưng không cần tìm điểm uốn thấp.
– Các NC cho thấy PEEP cao chỉ tác dụng với ARDS vừa và nặng có PaO2/FiO2 < 200.
– Hiện nay thống nhất dùng bảng phối hợp PEEP và FiO2 theo ARDS Network hoặc để mức PEEP cao nhất có thể cho đến khi Pplat = 28 – 30 cmH2O.
– Một số chuyên gia khuyên dùng PEEP 10 – 15 cmH2O trong vòng 48-96 giờ đầu của ARDS nếu các thông số khác như áp lực bình nguyên vẫn trong các giới hạn có thể chấp nhận được.
Thủ thuật huy động phế nang:
Mục đích: mở các phế nang đã bị xẹp bằng thủ thuật huy động phế nang (mở phổi) và
giữ cho các phế nang đã mở không xẹp lại bằng áp dụng PEEP tối ưu sau khi mở phổi.
Chỉ định:
– ARDS vừa và nặng.
– BN ARDS bị gián đoạn thở máy 1 thời gian: hút đờm, thay dây máy thở, vận chuyển…
Chống chỉ định:
– Rối loạn huyết động
– Rối loạn nhịp tim
– Tăng áp lực nội sọ
– COPD
– Tràn khí màng phổi
– Chống chỉ định dùng an thần, giãn cơ
Biện pháp: có nhiều cách thực hiện: CPAP với áp lực dương là 40cmH2O trong thời gian 40 giây, thở máy phương thức P – A/C với P = 20 và PEEP = 40 trong 120 giây hoặc P = 15, PEEP tăng dần từ 15 – 35, hoặc thở dài.
Chuẩn bị BN: cho BN thở hoàn toàn theo máy mới bắt đầu thủ thuật.
– Midazolam 5 mg x 1 ống tiêm tĩnh mạch (TM). Có thể tiêm mỗi 5 phút 1 ống hoặc dùng propofol.
– Morphin 10 mg x 1/2 ống TM hoặc dùng Fantanyl.
– Tracrium 4mg x 1 ống TM.
Phương pháp với thở máy P —A/C:
– Mode P – A/C: Pcontrol = 20 cmH2O, PEEP = 40 cmH2O
– Tần số hô hấp 10 lần/ph -Ti = 2.5 giây hoặc I/E = 1:1
– Tiến hành trong 120 giây
– Chú ý chỉnh giới hạn trên của alarm áp lực là 70 cmH2O nếu không máy sẽ báo động AL cao.
– Sau thủ thuật đưa về PEEP = 20 cmH2O, sau đó dò tìm PEEP tối ưu.
Phương pháp mở phổi tăng PEEP từ từ:
– Mode P – A/C: P control = 15cmH2O, tần số hô hấp 10 lần/ph, I:E = 1:1, FiO2 = 1.0, PEEP 15 cmH2O.
– Bắt đầu với PEEP = 15 → sau 5 – 6 nhịp thở → đưa PEEP lên 20 → sau 5 – 6 nhịp thở → đưa PEEP trở lại 15 → sau 5 – 6 nhịp thở → lại đưa PEEP lên 25 → sau 5 -6 nhịp → đưa trở lại 15 → sau 5 – 6 nhịp thở → đưa PEEP lên 30 → sau 5 – 6 nhịp thở → đưa PEEP trở lại 15 → sau 5 – 6 nhịp thở → lại đưa PEEP lên 35 → sau 5 -6 nhịp → lần này không đưa về 15 nữa, mà để PEEP = 20 → làm khí máu động mạch, nếu PaO2 + PaCO2 > 400mmHg (hoặc PaO2 > 350mmHg) thì coi như huy động phế nang thành công (chỉ còn < 5% các phế nang xẹp).
+ Nếu không thành công, làm lại huy động phế nang như trên nhưng PEEP không chỉ tăng đến 35 mà có thể tăng đến 40 hoặc 45. Nếu vẫn thất bại thì huy động phế nang ở tư thế nằm sấp.
Cách dò tìm PEEP tối ưu:
– Giảm PEEP từ 20 cmH2O (là mức PEEP sau thủ thuật huy động phế nang bằng cả 2 phương pháp) xuống từ từ, mỗi lần 1 cmH2O mỗi 5 phút để tìm điểm áp lực đóng phế nang (điểm AL mà phế nang xẹp lại), PEEP tối ưu chính là AL này cộng thêm 2 cmH2O
-Có 2 cách tìm điểm áp lực đóng phế nang:
+ Phương pháp oxy hóa máu tốt nhất: làm KMĐM mỗi lần giảm PEEP, tại mức PEEP có PaO2 giảm hơn 10% giá trị trước là điểm đóng phế nang, cộng 2 cmH2O là PEEP tối ưu.
+ Phương pháp compliance tốt nhất: xác định compliance tại mỗi mức PEEP, tại mức PEEP mà compliance giảm nhiều so giá trị trước đó là điểm đóng phế nang, cộng 2 cmH2O là mức PEEP tối ưu
– Trong khi tìm điểm AL đóng phế nang thì các phế nang sẽ bị xẹp lại nên sau khi đã xác định được PEEP tối ưu thì phải Mở Phổi lại rồi để PEEP ở mức PEEP tối ưu đã xác định.
– ARDS do nguyên nhân ngoài phổi (viêm tụy cấp…) thì PEEP tối ưu thường là 16 -18cm H2O trong mấy ngày đầu và 8 -12 cm H2O sau 1 -2 ngày.
Thở máy sau làm thủ thuật với các mục tiêu:
– Pplat < 30 cm H2O
– Vt = 6mL/kg PBW
– PEEP tối ưu như trên.
– FiO2 < 0.6
– Chấp nhận tăng CO2 (Permissive hypercapnia).
Chú ý:
– Nhắc lại thủ thuật khi thay đổi tư thế, khi ngắt mạch thở, khi hút đàm, khi cơ học phổi xấu hơn hoặc PaO2 lại tụt giảm.
– Kết thúc thủ thuật nếu:
+ SpO2 tụt giảm hơn .
+ MAP < 60
+ M < 60 hoặc > 20% so lúc đầu.
+ Loạn nhịp mới xẩy ra.
Cai máy:
– Đánh giá cai máy hàng ngày giữa 8-12 giờ sáng.
– Bắt đầu cai máy bằng chế độ thở hỗ trợ áp lực khi BN có đủ các tiêu chuẩn sau:
+ FiO2 < 0,4 và PEEP < 8 cmH2O.
+ Hiện tại không dùng thuốc ức chế thần kinh cơ.
+ Có gắng sức hít vào rõ ràng (giảm tần số thở xuống < 50% tần số thở hiện tại trong 5 phút để phát hiện gắng sức hít vào của BN).
+ Huyết áp tâm thu > 90mmHg mà không dùng vận mạch.
Một số vấn đề với thông khí cơ học cho BN ARDS:
Có nên thử nghiệm thở máy không xâm lấn trước khi quyết định đặt nội khí quản? lựa chọn phương thức thở máy xâm lấn nào? Làm gì nếu giảm oxy máu dai dẳng?
Làm sao lựa chọn PEEP tối ưu? Có nên dùng giãn cơ hay không?
Thở máy không xâm lấn:
– Có thể cho BN ARDS thử nghiệm thở máy không xâm lấn trong trường hợp: BN tỉnh, huyết động ổn định, mức độ ARDS không nặng (PaO2/FiO2 > 200), có thể dung nạp thở máy qua mask, tự bảo vệ đường thở được.
– Cài đặt và chọn lựa lúc bắt đầu:
+ Đặt EPAP = 4cmH2O, điều chỉnh FiO2 duy trì SaO2 hoặc SpO2 > 92%.
+ IPAP = 8cmH2O, điều chỉnh IPAP để đạt được VTe khoảng 6-8mL/kg (Chú ý,
VTe phụ thuộc vào chênh lệch giữalPAP và EPAP; PS = IPAP – EPAP).
+ Theo dõi BN, đánh giá chức năng sống, SaO2, SpO2, VTe.
+ Tiếp tục giữ nguyên các thông số đã đặt, theo dõi sát BN nếu BN thấy dễ chịu khi thở máy, có: tần số thở < 30 lần/phút; tần số tim không tăng quá 20% so với tần số ban đầu; không loạn nhịp tim; không còn cảm giác khó thở, không co kéo cơ hô hấp phụ; Vte duy trì từ 6-8 ml/kg; SpO2 > 92%.
– Nếu SpO2 < 92%, tăng FiO2 từng mức 10% cho tới 100%. Nếu đã tăng FiO2 lên tới 100% mà SpO2 vẫn < 92%, tăng EPAP mỗi lần 2cmH2O (tối đa lên tới 10cmH2O).
Chú ý khi tăng EPAP, phải tăng đồng thời IPAP sao cho IPAP luôn hơn EPAP 4cmH2O.
– Nếu BN có co kéo cơ hô hấp, Vte thấp < 6ml/kg, mệt cơ, PaCO2 bắt đầu tăng hoặc không giảm, trước tiên phải kiểm tra xem độ khít của mặt nạ. Nếu không cải thiện tăng IPAP dần lên, mỗi lần 2cmH2O (tối đa lên tới 20 cmH2O) và đánh giá lại lâm sàng sau 30 phút. Chú ý khi tăng IPAP, Vte phải tăng theo.
– Nếu tình trạng BN cải thiện; SpO2 > 92%, duy trì các thông số, điều chỉnh mức FiO2 thấp nhất có thể được và xem xét khả năng cai máy thở.
– Nếu tình trạng BN xấu đi: thở nhanh > 30 lần/phút, SpO2 < 90%, tần số tim tăng >
20%, IPAP = 20 và EPAP = 10, rối loạn ý thức, rối loạn huyết động thì phải đặt nội khí quản ngay.
Lựa chọn phương thức thở:
– Trong ARDS, để theo chiến lược Vt thấp thì nên chọn thể tích (Volume Cotrol,
VCV hoặc V – A/C), tuy nhiên, cũng có thể dùng phương thức áp lực (Pressure Control, PCV hoặc P – A/C) miễn là tuân theo chiến lược Vt thấp.
– Thở máy phương thức PCV:
+ PC điều chỉnh đạt mục tiêu Vt thấp = 6mL/kg PBW.
+ Điều chỉnh FiO2 và PEEP sao cho đạt được mục tiêu oxy hóa. Có thể điều chỉnh theo bảng ARDS Network hoặc chọn PEEP tối ưu rồi điều chỉnh FiO2.
+ Yêu cầu PC + PEEP < 30cmH2O và càng thấp càng tốt.
– Các phương thức thở máy hiện đại khác như APRV (airway pressure release ventilation) hoặc HFV ( high frequency ventilation) có thể có lợi trong các trường hợp thở máy theo qui ước thất bại. Tuy nhiên, chưa có bằng chứng đủ để dùng các phương thức này thường qui.
Giảm oxy máu dai dẳng:
Ngoài các biện pháp thở máy như trên, nếu thất bại, có thể áp dụng biện pháp kéo dài thời gian hít vào, thậm chí I/E đảo ngược. Nhược điểm là thời gian thở ra bị thu ngắn gây ra bẫy khí, Auto – PEEP, tổn thương phổi, rối loạn huyết động, đồng thời BN cũng phải dùng an thần, giảm đau, giãn cơ mạnh.
4.1.3 Các điều trị khác tư thế bệnh nhân
Vì tổn thương phổi phân bố không đều ở các BN ARDS, thay đổi tư thế có thể cải thiện oxy hóa máu bằng cách gia tăng tưới máu ở các vùng phổi được thông khí.
BN có thể nằm nghiêng phải hoặc trái hay nằm sấp. Duy trì ở tư thế nằm sấp 18-20 giờ mỗi ngày.
❖ Chống chỉ định nằm sấp khi:
– Có vết thương hở/bỏng ở mặt trước của cơ thể
– Có gãy xương không vững
– Gãy cột sống không vững
– Tăng áp lực nội sọ
– Huyết động không ổn định
– Cần thận trọng nếu bệnh nhân được mở khí quản, đặt ống dẫn lưu màng phổi, béo phì, cổ trướng
An thần, giảm đau, giãn cơ:
Bảng điểm an thần Ramsay
|
Điểm |
Mức độ ý thức |
|
1 |
Tỉnh, hốt hoảng, kích thích, vật vã |
|
2 |
Tỉnh, hợp tác, có định hướng, không kích thích |
|
3 |
Tỉnh, chỉ đáp ứng khi ra lệnh |
|
4 |
Ngủ, đáp ứng nhanh khi bị kích thích đau, nói to |
|
5 |
Ngủ, đáp ứng chậm khi bị kích thích đau, nói to |
|
6 |
Ngủ sâu, không đáp ứng |
– Dùng an thần (benzodiazepine) – giảm đau (nhóm morphin) hoặc phối hợp an thần, giảm đau và giãn cơ là rất cần thiết cho BN ARDS phải thở máy. Có thể dùng propofol thay thế cho benzodiazepine.
– An thần, giảm đau nên tiêm ngắt quãng hoặc truyền liên tục nhưng cho nghỉ 2 – 3 giờ hàng ngày.
– Nên dựa vào thang điểm Ramsay (mục tiêu 4 – 5 điểm) hoặc RASS (Richmond Agitation-Sedation Scale) khi dùng an thần.
– Nên dùng giãn cơ cho BN ARDS có PaO2/FiO2 < 120 và dùng trong 48 giờ.
– An thần, giảm đau, giãn cơ cần giảm liều và dừng đúng lúc khi bệnh tiến triển tốt lên để cai máy thở kịp thời và bỏ máy sớm nhất có thể.
Dịch truyền
Phải kiểm soát dịch chặt chẽ với mục tiêu duy trì CVP ≤ 4 mmHg (5cmH2O) nhưng không gây tụt HA và không gây giảm tưới máu cơ quan. Nên cân nhắc phối hợp dung dịch albumin và furosemid để cải thiện oxy hoá, huyết động và cân bằng dịch.
Nếu bệnh nhân tăng cân, cân bằng dịch dương, dùng lợi tiểu quai tiêm tĩnh mạch với liều thích hợp để điều chỉnh kịp thời đưa bệnh nhân trở về cân nặng ban đầu. Kháng sinh
Chỉ sử dụng khi có nhiễm khuẩn, không dùng kháng sinh dự phòng.
Dinh dưỡng
Cần cung cấp dinh dưỡng đầy đủ, nếu được nuôi ăn liên tục tốt hơn ngắt quãng vì tình trạng liệt dạ dày ruột thường xảy ra.
Sử dụng steroid:
Trong ngày 1-7, lý tưởng là ≤ 72 giờ:
– Cho methylprednisolone 1mg/kg bolus tĩnh mạch, sau đó dùng liều lmg/kg/ngày truyền tĩnh mạch liên tục trong 14 ngày.
– Nếu Bn đang dùng thuốc giãn cơ, trì hoãn sử dụng steroid tới khi không cần dùng đồng thời với thuốc giãn cơ.
– Nếu không thấy có lợi ích rõ rệt về thực thể hay hình ảnh X-quang sau khi dùng steroid 3-5 ngày thì ngưng.
– Sau 14 ngày hoặc sau khi rút được ống NKQ thành công, giảm liều xuống 0,5mg/kg/ngày tiêm TM và tiếp tục dùng thuốc trong 7 ngày, sau đó giảm liều xuống còn 0,25mg/kg/ngày tiêm TM trong 7 ngày tiếp, sau đó ngưng dùng thuốc.
Ngày 7-14, nếu steroid không được bắt đầu dùng sớm:
Lợi ích không chắc chắn, song ở các trường hợp chọn lọc có thể thử áp dụng cùng
phác đồ như trên. Nếu không thấy có lợi ích rõ rệt về thực thể hay hình ảnh X-quang
sau khi dùng thuốc 3-5 ngày thì ngưng.
Sau 14 ngày: có lẽ steroid không có vai trò gì trong trường hợp này.
4.2 Điều trị nguyên nhân
– Tùy theo nguyên nhân gây khởi phát ARDS mà chúng ta điều trị đặc hiệu.
– Ví dụ: viêm phổi nặng, sốc nhiễm khuẩn thì điều trị kháng sinh tích cực.
5 Phòng bệnh:
– Điều trị tích cực, mạnh mẽ ngay từ đầu các nguyên nhân có thể dẫn đến ARDS: viêm tụy cấp, viêm phổi nặng…
– Tránh viêm phổi hít.
Tài liệu tham khảo:
1. Phác đồ Bệnh viện Bạch Mai (2012). Hội chứng suy hô hấp cấp tiến triển. Trang 83-85.
2. Phác đồ Bệnh viện Chợ Rẫy (2012). Trang Hội chứng suy hô hấp cấp nguy kịch. Trang 55-61.
3. Bedient TJ; Kollef MH (2012). Acute Lung Injury and the Acute Respiratory Distress Syndrome. Washington Manual of Critical Care, The, 2nd Edition, p58-66.
4. Siegel MD, Hyzy RC (2014). Mechanical ventilation in acute respiratory distress syndrome. UpToDate,Inc. Release: 22.2 – C22.40